Формула етанолу: хімічна структура та властивості
Формула етанолу є однією з найбільш відомих у світі органічних сполук: C2H5OH. Це класичний представник спиртів, який має ключове значення як в біологічних, так і в промислових процесах. Етанол, також відомий як етиловий спирт, є компонентом алкогольних напоїв, розчинником, пальним і сировиною для синтезу багатьох хімічних продуктів.
Хімічна структура етанолу
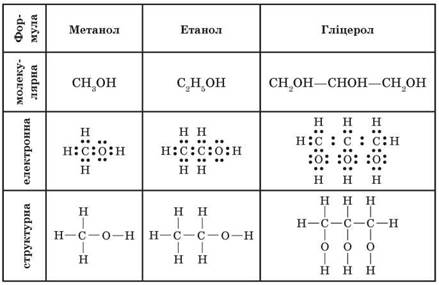
Етанол є представником класу органічних сполук, які називаються спиртами. Основою його структури є двувуглецевий ланцюжок з однією гідроксильною групою (-OH) на кінці одного з атомів вуглецю.
- Вуглецевий ланцюг: Етанол містить два атоми вуглецю, які об’єднані ковалентним зв’язком. Така структура визначає його фізичні та хімічні властивості.
- Гідроксильна група: -OH група зумовлює полярність молекули етанолу, що забезпечує високу розчинність у воді та інших полярних розчинниках.
Хімічні та фізичні властивості
Формула етанолу, C2H5OH, пояснює деякі з його ключових властивостей. Нижче наведена таблиця з основними характеристиками етанолу:
| Властивість | Значення |
|---|---|
| Молекулярна маса | 46.07 г/моль |
| Температура кипіння | 78.37°C |
| Температура замерзання | -114.1°C |
| Густина | 0.789 г/см3 |
Використання етанолу
Етанол має широкий спектр застосувань у різних галузях:
- Алкогольні напої: Етанол є основним активним інгредієнтом у пиві, вині та спиртних напоях, який забезпечує їх психоактивні властивості.
- Паливо: Використовується як біопаливо в транспорті; часто змішується з бензином для зменшення викидів забруднюючих речовин.
- Промислове застосування: Служить розчинником у фармацевтичній, косметичній та хімічній промисловості.
Реакції за участю етанолу
Етанол може вступати в різні хімічні реакції, демонструючи властивості як кислоти, так і основи. Деякі з найважливіших реакцій за участю етанолу включають:
- Естаріфікація — реакція з кислотами для утворення естерів.
- Оксидація — перетворення в ацетальдегід, а згодом в кислоту.
Розуміння формули етанолу та його властивостей є надзвичайно важливим як для науки, так і для промисловості. Це надає можливість не лише використовувати його в різних технологічних процесах, але й розробляти нові методи і рішення, що відповідають екологічним та економічним вимогам сучасності.