Сірчана кислота: формула, властивості та застосування
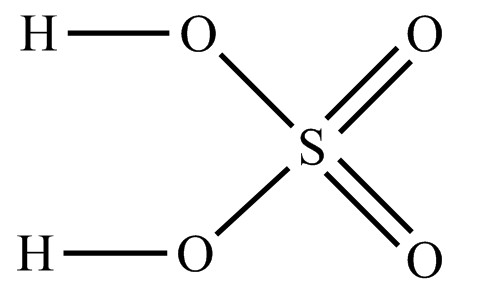
Сірчана кислота, формула якої H2SO4, є одним з найважливіших і широко використовуваних промислових хімічних сполук. Її значення у хімічній промисловості, агрохімії та багатьох інших галузях важко переоцінити. У цій статті ми розглянемо основні властивості, методи отримання та застосування сірчаної кислоти.
Основні властивості сірчаної кислоти
- Хімічна формула: H2SO4
- Молярна маса: 98.079 г/моль
- Щільність: 1.84 г/см3 при 25°C
- Температура кипіння: 337°C
- Температура плавлення: 10°C
Сірчана кислота – безбарвна рідина з високою в’язкістю і корозійною активністю. Вона має сильні гігроскопічні властивості, тобто активніше поглинає вологу з повітря, що може спричиняти корозію в навколишньому середовищі.
Методи отримання сірчаної кислоти
Найпоширенішим методом виробництва сірчаної кислоти є контактний процес. Його основні етапи такі:
- Спалювання сірки або сульфідних руд з утворенням діоксиду сірки (SO2).
- Окиснення SO2 до триоксиду сірки (SO3) в присутності каталізатора (найчастіше ванадій оксид).
- Абсорбція SO3 водою з утворенням сірчаної кислоти:
| SO3(г) + H2O(р) → H2SO4(р) |
Застосування сірчаної кислоти
Сірчана кислота має широкий спектр застосувань у різних галузях промисловості:
- Хімічна промисловість: Використовується для виробництва різноманітних кислот, у тому числі фосфорної і хлоридної, а також для синтезу барвників і детергентів.
- Агрохімія: Використовується у виробництві добрив, таких як сульфат амонію та суперфосфат.
- Нафтова промисловість: Використовується для очищення нафтопродуктів і отримання високоякісного пального.
- Металургія: Використовується для вилужування металів, зокрема при виробництві міді та цинку.
Сірчана кислота, формула якої ми розглянули, залишається однією з життєво важливих хімічних сполук у сучасному світі. Її багатогранні властивості та широке застосування підкреслюють значення цієї кислоти у підтримці технологічного і економічного прогресу.